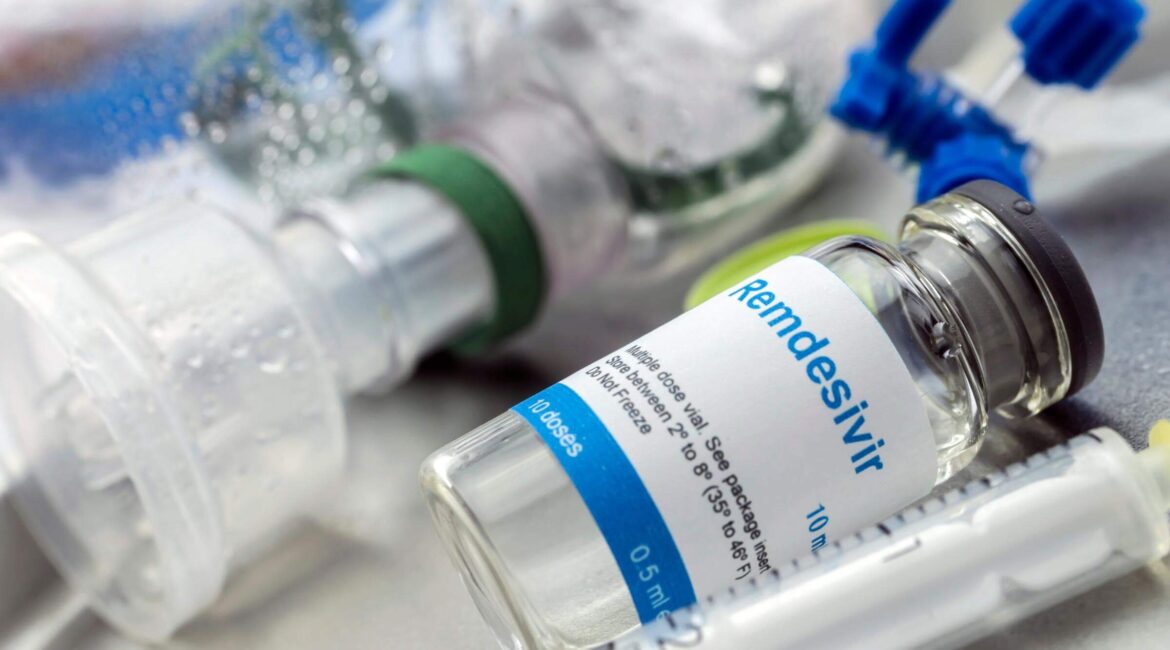
Organizata më prestigjioze e kujdesit intensiv këshillon mospërdorimin e remdesivir te pacientët me COVID-19 të rëndë. Remdesivir është një prodrogë me një strukturë analoge me atë të nukleotideve. Metabolizohet si një analog i adenozinë trifosfatit, i cili inhibon ARN polimerazën virale të varur nga ARN, duke nxitur përfundim të parakohshëm të transkriptimit të ARN-së. Kjo gjetje është parë në pjata petri dhe eksperimente laboratorike në linja qelizore. Remdesivir, gjithashtu (i njohur ndryshe si Veklury) dhe deksametazoni janë të vetmet barna të cilat janë autorizuar (remdesiviri me kusht!) deri tani.
Hulumtimi më i madh dhe më serioz (deri tani), i njohur si SOLIDARITY trial zbuloi se remdesivir ka pak ose aspak impakt mbi kursin e COVID-19, duke qartësuar situatën për përdorimin e këtij bari. Më tej, në prononcimin zyrtar e sotëm zyrtar (15.11.2020 – këtu), Presidenti i Shoqatës Europiane të Mjeksësisë së Shërbimit Intensiv (ESCIM), Prof. Dr. Jozef Kesecioglu tha se ‘remdesivir tashmë klasifikohet si një bar që nuk duhet të përdoret në trajtimin rutinë te pacientët me COVID-19’. Kjo deklaratë pritet të mbështetet nga një hulumtim i ri që do të publikohet në Janar 2021 – botim ky që është duke u përgatitur prej ESCIM dhe Shoqërisë së Mjekësisë së Kujdesit Kritik.
Sipas një botimi shkencor të publikuar në presitiogjiozen Science (këtu), tregohet qartë se kompania Gilead (që prodhon barin remdesivir) i dinte rezultatet të SOLIDARITY trial dhe Agjensia Europiane e Barnave (EMA) ka kërkuar një ri-vlerësim të të gjithë të dhënave për remdesivir, pas daljes së rezulateve të SOLIDARITY trial. ‘Kjo situatë nuk përbën fare një situatë të këndshme për Gilead, kompaninë që prodhon remdesivir’ ka deklaruar kryeredaktori i Medscape, Dr, Eric Topol.
SOLIDARITY trial (këtu) u realizua në 30 vende dhe kishte një numër pacientësh prej 2750 individësh në grupin e remdesivir. Një numër ky pothuajse tri herë më i madh se të gjitha provat klinike të publikuara deri tani për këtë bar të marra së bashku. Ky studim demonstroi se remdesivir ka pak ose aspak efekt në:
- Uljen e vdëkshmërisë,
- Kohëzgjatjen e hospitalizimit ose
- Nevojshmërisë për ventilatorë
Mirëpo cilat kanë qenë provat e deritanishme që kanë mbështetur aprovimin me kusht nga EMA dhe aprovimin emergjent nga FDA? Duke u bazuar në burimet e prestiogjiozes Science (këtu), është e rëndësishme të theksohet se FDA nuk është konsultuar me grupin e ekspertëve përkatës.
Në këto momente është gjithashtu e rëndësishme të njohim anën tjetër të historisë: remdesivir tashmë i është nënshtruar një hetimi nga Komiteti i Sigurisë së EMA, për shkak të efekteve anësore kryesisht në formën e dëmtimeve akute të veshkave te disa nga pacientët që e kanë marrë barin (që arrijnë deri në 24.6% të tyre këtu).
Provat klinike të deritanishme për remdesivir nuk kanë treguar efikasitet në uljen e vdekshmërisë. Konkretisht NIAID trial (ACT-1) nuk tregoi ulje të vdekshmërisë deri në ditën e 14-të (HR=0.7 (0.47-1.04, pa sinjifikancë: P>0.05). Gjithashtu u vunë re efekte serioze anësore të raportuara në 24.6% të pacientëve në grupin e pacientëve të trajtuar me remdesivir (këtu). I vetmi tregues statistikor i përmirësuar modestisht ishte reduktimi i kohës mediane të hospitalizimit tek ata pacientë të cilët ishin hospitalizuar – një tregues jo shumë i lehtë për t’u interpretuar.
Një tjetër provë klinike e randomizuar në pacientë me paraqitje të COVID-19 të moderuar (këtu), që krahasoi remdesivirin me kujdesin standard, nuk gjeti ndryshim sinjifikant ndërmjet shpërndarjes së statusit klinik në ditën 11 grupi i pacientëve që u trajtuan 10 ditë me remdesivir, krahasuar me kujdesin standart (p=0.18).
Në një provë tjetër klinike në pacientë me paraqitje të COVID-19 të rëndë, nuk u gjet një ndryshim sinjifikant ndërmjet kursit 5- dhe 10-ditor të trajtimit me remdesivir (këtu). Për më tepër, ky studim nuk kishte as grup kontrolli!
Një tjetër provë klinike e randomizuar që vlerësoi efikasitetin e remdesivir për 10 ditë kundrejt palcebos tek të rriturit me COVID-19 (në 10 spitale të ndryshme në Vuhan të Kinës), tregoi se remdesivir nuk kishte efekt sinjifikant mbi kohën e përmirësimit klinik (HR=1.23, 95%CI: 0.87-1.75). Megjithatë ky studim kishte fuqi shumë të vogël studimi dhe u ndërpre pasi rastet në Vuhan u ulën, gjë që e bën hulumtimin jo-konkluziv (këtu).
Më tej, ka pasur një seri rast-raportimesh mbi remdesivir me rezultate konfliktuale (këtu, këtu, këtu, këtu dhe këtu), por në hierarkinë e evidencave këto lloj studimesh janë niveli i ulët i evidencave.
Konsiderata mbi toksicitetin dhe monitorimin e efekteve anësore
Gjetjet më të shpeshta laboratorike që janë vënë re tek pacientët që kanë marrë remdesivir në provat klinike të randomizuara janë transaminazat e shtuara (AST, ALT), dëmtimet akute të veshkave, flevit, konstipacion, dhimbje koke dhe të përziera. Remdesiviri bashkëformulohet me sulfobutil eter β-ciklodextrin (i njohur shkurt si SBECD), kështu që ekziston një rrezik për akumulim në insuficiencën renale, gjë që promovon më tej dëmtime të veshkave, të ngjashme me administrimin e voriconazole. Nëse remdesivir përdoret në prova klinike, në pacientë me dëmtime të veshkave, përfitimet e pritshme duhet të tejkalojnë rreziqet potenciale në gjykimin klinik, përpara fillimit të provës klinike (këtu). Nëse remdesivir përdoret në rastet me eGFR<30 mL/min, gjatë provës klinike, rekomandohet forma e tij pluhur, duke qenë se ka më pak përmbajtje SBECD krahasuar me formën e lëngshme (3 gram kundrejt 6 gram respektivisht).
Një informacion kyç vjen nga një studim rast-raportim nga Holanda ku përshkruhet një pacient me COVID-19, i cili pas administrimit të remdesivir zhvilloi hepatotoksicitet akut, gjë që mund të ketë ardhur si pasojë e ndërveprimit me inhibitorët e P-glikoproteinës (P-gp), amiodaronit dhe klorokuinës. Remdesivir është një substrat i P-gp in vitro, por ky ndërveprim (reaksion) potencial ka nevojë për hulumtime të mëtejshme, në mënyrë që të informohet më qartë praktika klinike (këtu).
Në përfundim, duke marrë parasysh udhërrëfyesin zyrtar për trajtimin e COVID-19, të botuar nga Organizata Botërore e Shëndetësisë (këtu), përditësimin shkencor të Ekipit të zgjeruar anti-COVID-19 të HEDA Albania (këtu) të realizuar nga bashkëpunimi i 25 shkencëtarëve e studiuesve shqiptarë nga Shqipëria dhe Kosova nuk rekomandohet përdorimi i Remdesivir jashtë kontekstit të provave klinike të randomizuara.